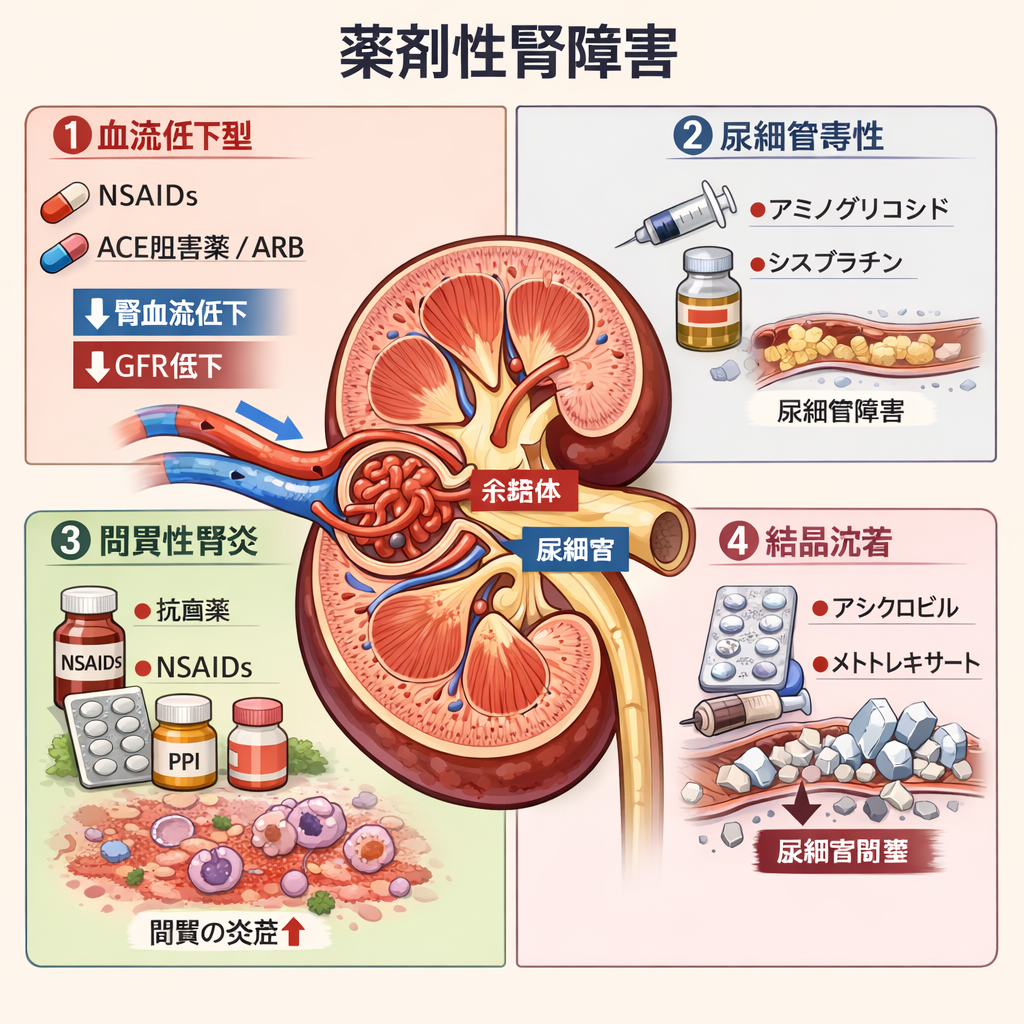
薬剤性腎障害
通常の状態
腎前性腎障害
血流の問題
腎性腎障害
腎臓の問題
腎後性腎障害
尿の通り道の問題
腎前性腎障害(Prerenal Acute Kidney Injury)
定義
腎臓自体には器質的な障害がないが、腎血流の低下によってGFRが低下する状態。
急性腎障害(AKI)の中で最も頻度が高いタイプです。
病態(基本メカニズム)
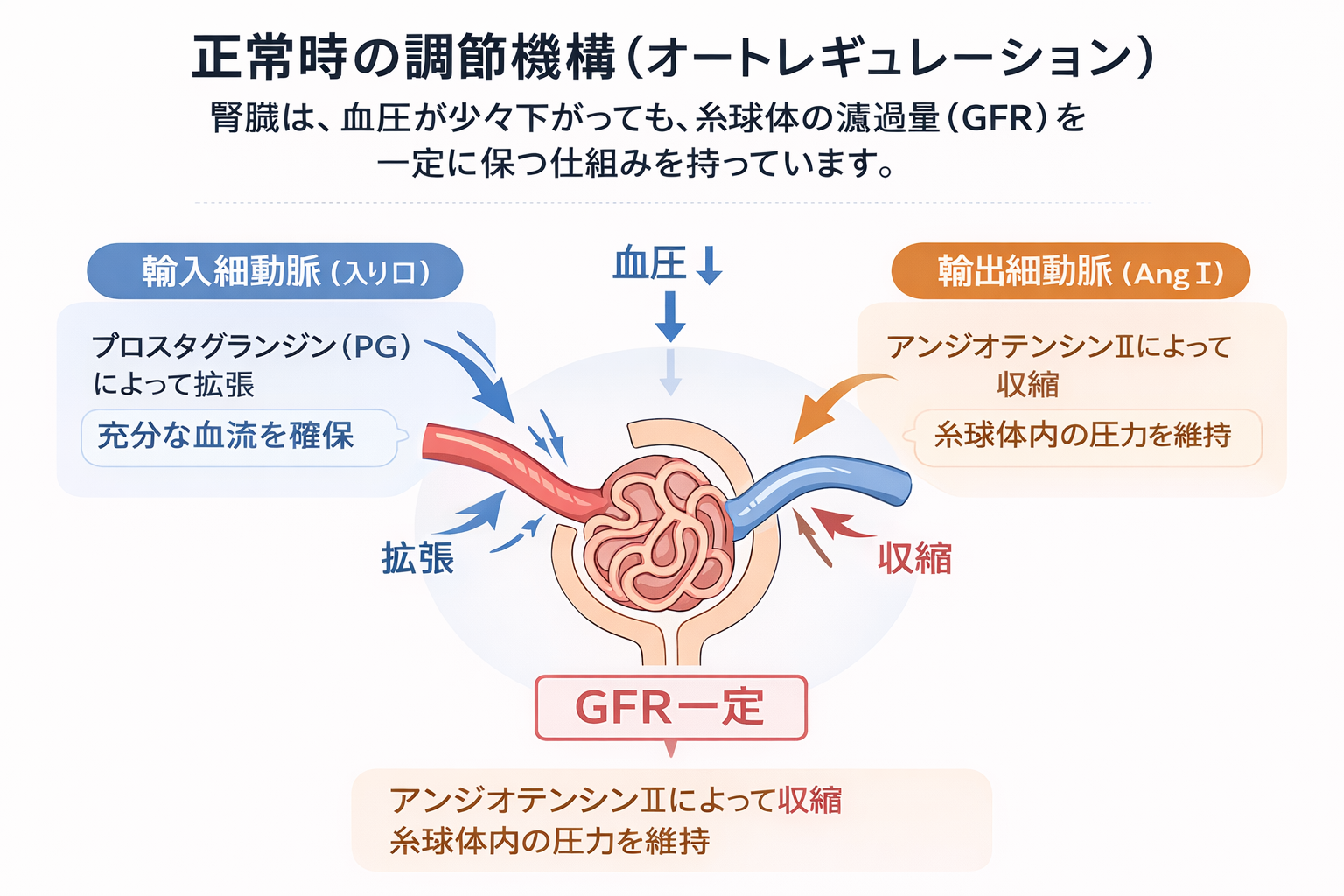
腎臓は通常、血圧が多少低下しても オートレギュレーション によりGFRを維持します。
①輸入細動脈(afferent arteriole)
- プロスタグランジン(PG)
→ 血管拡張
→ 腎血流を維持
②輸出細動脈(efferent arteriole)
- アンジオテンシンⅡ
→ 血管収縮
→ 糸球体内圧を維持
これにより GFRを保つ仕組み があります。
しかし
- 循環血液量低下
- 心拍出量低下
- 血管収縮
などが起こると
腎血流低下 → GFR低下 → 腎前性AKI
になります。
主な原因
①循環血液量低下
- 脱水
- 出血
- 下痢・嘔吐
- 利尿薬
②心拍出量低下
- 心不全
- 心筋梗塞
- 重症不整脈
③血管拡張・分布異常
- 敗血症
- 肝硬変
薬剤性の腎前性AKI
薬剤によって オートレギュレーションが破綻 することがあります。
| 薬剤 | 作用 | 結果 |
|---|---|---|
| NSAIDs | PG合成阻害 | 輸入細動脈収縮 |
| ACE阻害薬 / ARB | AngⅡ抑制 | 輸出細動脈拡張 |
| 造影剤 | 血管収縮 | 腎髄質血流低下 |
| 利尿薬 | 循環血液量低下 | 腎血流低下 |
特に有名なのが
トリプルワーミー
- NSAIDs
- ACE阻害薬 / ARB
- 利尿薬
→ 急性腎障害のリスク
検査所見(腎前性の特徴)
| 指標 | 所見 |
|---|---|
| BUN/Cr | 20以上 |
| FENa | 1%未満 |
| 尿浸透圧 | 高値 |
| 尿Na | 低値 |
理由
→ 腎臓が 水とNaを再吸収しているため
腎前性AKIの重要ポイント
早期に改善すれば腎機能は回復する
しかし
腎血流低下が続くと
急性尿細管壊死(ATN) → 腎性AKI
へ進行します。
腎性腎障害(Renal / Intrinsic Acute Kidney Injury)
定義
腎臓そのもの(糸球体・尿細管・間質・血管)に障害が起こり、腎機能が低下する状態
急性腎障害(AKI)の中では
腎前性の次に多いタイプです。
腎性腎障害の分類
腎臓のどこが障害されるかで分類します。
| 部位 | 疾患 |
|---|---|
| 糸球体 | 糸球体腎炎 |
| 尿細管 | 急性尿細管壊死(ATN) |
| 間質 | 急性間質性腎炎 |
| 腎血管 | 血管炎・血栓 |
最も多い原因
急性尿細管壊死(ATN)
主な原因
①虚血
- 腎前性AKIが持続
- 敗血症
- 手術
②腎毒性
薬剤例
| 薬剤 | 例 |
|---|---|
| アミノグリコシド | ゲンタマイシン |
| 抗癌薬 | シスプラチン |
| 造影剤 | ヨード造影剤 |
| 抗真菌薬 | アムホテリシンB |
| 抗ウイルス薬 | アシクロビル |
機序
→ 尿細管上皮細胞の障害
急性間質性腎炎(AIN)
薬剤アレルギーが原因
代表薬
- 抗菌薬(ペニシリン)
- NSAIDs
- PPI
特徴
- 発熱
- 発疹
- 好酸球増加
腎性AKIの検査所見
| 指標 | 所見 |
|---|---|
| BUN/Cr | 10〜15程度 |
| FENa | 2%以上 |
| 尿Na | 高値 |
| 尿沈渣 | 円柱 |
理由
→ 尿細管が壊れて
Na再吸収ができない
腎前性との違い(重要)
| 腎前性 | 腎性 | |
|---|---|---|
| 原因 | 腎血流低下 | 腎組織障害 |
| FENa | <1% | >2% |
| BUN/Cr | >20 | 10–15 |
| 可逆性 | 早期で回復 | 回復に時間 |
腎後性腎障害(Postrenal Acute Kidney Injury)
定義
尿の通り道(尿路)が閉塞することで尿が排出できなくなり、腎機能が低下する状態。
急性腎障害(AKI)の3分類のひとつで、
尿の出口側の問題で起こります。
病態(メカニズム)
通常の尿の流れ
どこかが閉塞すると
長時間続くと
水腎症(hydronephrosis) → 腎実質障害に進行します。
主な原因
①前立腺疾患(高齢男性で多い)
- 前立腺肥大
- 前立腺癌
→ 尿道を圧迫
②尿路結石
- 尿管結石
- 腎結石
→ 急激な閉塞
③腫瘍
- 膀胱癌
- 子宮癌
- 前立腺癌
- 大腸癌
→ 尿管圧迫
④神経因性膀胱
- 脊髄損傷
- 糖尿病神経障害
→ 排尿できない(尿閉)
⑤薬剤による尿閉
| 薬剤 | 機序 |
|---|---|
| 抗コリン薬 | 排尿筋抑制 |
| 三環系抗うつ薬 | 抗コリン作用 |
| 抗ヒスタミン薬 | 抗コリン作用 |
臨床での特徴
疑うポイント
- 尿量低下
- 排尿困難
- 下腹部膨満
- 尿閉
- 高齢男性
検査
最も重要なのは
超音波(エコー)
確認する所見
- 水腎症
- 膀胱内尿貯留
- 尿管拡張
治療
基本は 閉塞解除
| 原因 | 治療 |
|---|---|
| 尿閉 | 導尿・カテーテル |
| 尿管閉塞 | 尿管ステント |
| 結石 | 砕石 |
| 腫瘍 | 手術 |
Sales GTM, Foresto RD. Drug-induced nephrotoxicity. Rev Assoc Med Bras (1992). 2020 Jan 13;66Suppl 1(Suppl 1):s82-s90. doi: 10.1590/1806-9282.66.S1.82. PMID: 31939540. https://pubmed.ncbi.nlm.nih.gov/31939540/
Title(英語)
Drug-induced nephrotoxicity
Title(日本語)
薬剤誘発性腎毒性
Journal Name & Publication Year
Revista da Associação Médica Brasileira(2020年)
First and Last Authors
• First Author: Gabriel Teixeira Montezuma Sales
• Last Author: Renato Demarchi Foresto
First Affiliations
Universidade Federal de São Paulo, São Paulo, Brazil
Abstract(要旨)
急性腎障害(AKI)は非常に一般的な診断であり、重症患者の最大60%に認められる。薬剤毒性はAKIの第3位の原因である。薬剤性腎毒性は、薬剤によって直接または間接的に引き起こされる腎障害と定義され、主な臨床像として以下がある。
• 急性腎不全
• 尿細管障害(tubulopathy)
• 糸球体障害(glomerulopathy)
代表的な原因薬剤として以下が挙げられる。
GFR低下を起こす薬剤
• 非ステロイド性抗炎症薬(NSAIDs)
• バンコマイシン
• アミノグリコシド系抗生物質
• シスプラチン
• メトトレキサート
尿細管障害を起こす薬剤
• アンホテリシンB
• ポリミキシン
• テノホビル
糸球体障害を起こす薬剤
• VEGF阻害薬
• ビスホスホネート
• 免疫チェックポイント阻害薬
早期診断とリスク因子の把握、毒性薬剤の中止または代替が重要である。
Background(背景)
AKIの発生率は近年増加しており、その理由として以下が挙げられる。
• 高齢化
• 慢性腎臓病(CKD)の増加
• 糖尿病の増加
• 腎毒性を持つ薬剤使用の増加
腎臓は薬物や代謝産物の排泄を担うため、糸球体や尿細管が高濃度の薬物に曝露されやすい。そのため薬剤による腎障害が生じやすい。
薬剤性腎障害の疫学では、AKIの約25%が薬剤関連とされる。また、約20%の症例では腎代替療法が必要となり、特に発展途上国では死亡率が60%以上になることが報告されている。
Methods(方法)
本論文は主にレビュー論文であり、薬剤性腎毒性の以下の項目について既存研究を基に整理している。
• 発症機序
• 危険因子
• 主要薬剤
• 臨床症候群
• 予防・治療戦略
さらに、腎毒性の早期診断に有用なバイオマーカーについてもまとめている。
Results(結果)
1. 腎毒性の主な危険因子
代表的なリスク因子
• 高齢
• 低血容量
• 慢性腎臓病
• 糖尿病
• 心疾患
• 高用量薬物
• 低血圧
• 複数の腎毒性薬剤の併用
2. 腎障害のタイプ
薬剤性腎障害は主に以下に分類される。
① GFR低下・急性腎障害
例
• NSAIDs
• バンコマイシン
• アミノグリコシド
• シスプラチン
• メトトレキサート
② 尿細管障害
例
• アンホテリシンB
• ポリミキシン
• テノホビル
③ 糸球体障害
例
• VEGF阻害薬
• ビスホスホネート
• 免疫チェックポイント阻害薬
3. 代表的薬剤の腎毒性
NSAIDs
• プロスタグランジン阻害
• 輸入細動脈収縮
→ GFR低下
バンコマイシン
• AKI発症率 5〜15%
• リスク
◦ 用量 >4 g/day
◦ 投与期間 >14日
◦ 血中濃度上昇
アミノグリコシド
• 高リスク患者で最大50%のAKI
シスプラチン
• AKI発症率 34%(800人以上のコホート)
メトトレキサート
• 高用量(>500 mg/m²)でAKI
• 発症率 最大12%
4. 新しい腎障害バイオマーカー
早期診断候補
• KIM-1
• β2ミクログロブリン
• Clusterin
• Cystatin C
これらはクレアチニン上昇より早く検出可能とされる。
Discussion(考察)
近年、感染症や癌治療の進歩により多くの新薬が登場したが、その副作用として腎毒性が依然として大きな問題である。
腎毒性管理の中心は
1. 早期診断
2. 危険因子の評価
3. 毒性薬剤の減量または中止
さらに以下の戦略が重要とされる。
• 血中薬物濃度モニタリング
• 腎機能に基づく投与量調整
• 低血容量の補正
• 腎毒性薬剤併用の回避
電子カルテによる腎毒性アラートシステムも有効とされている。
Novelty compared to previous studies(新規性)
本論文の特徴
1. 薬剤ごとの腎障害タイプを体系的に整理
2. 尿細管・糸球体など病態別に分類
3. 新規バイオマーカーの臨床応用の可能性を提示
4. 薬剤併用による相乗毒性(synergistic nephrotoxicity)を強調
特に薬剤の**病態別分類(AKI・tubulopathy・glomerulopathy)**は臨床診断に有用である。
Limitations(限界)
• レビュー論文であり新規臨床試験データは含まれていない
• 発症率は研究によって差がある
• バイオマーカーはまだ臨床標準ではない
Potential Applications(応用可能性)
臨床応用
1. 腎毒性薬剤のリスク評価
2. 抗菌薬・抗癌剤使用時の腎機能モニタリング
3. 腎障害の早期診断バイオマーカー開発
4. 薬剤投与量調整アルゴリズムの改善
5. 薬剤性AKI予防プログラムの設計
特にICUや腫瘍治療では、薬剤性腎障害の予防に直接応用可能である。
SciDraft (Japanese)を利用すると、研究室での進捗スライドや作成済みの研究計画書から論文ドラフトを執筆することが可能です。
上記リンク先記事にURLが載っているので、ぜひお試しください!
また、Readableを利用すると、論文PDFのレイアウトを保ったまま日本語への翻訳が可能です。
クーポンコード"PaperInterpreter"の入力で1ヶ月間フリートライアルできるので、こちらもぜひお試しください😊
- •
First Author: Gabriel Teixeira Montezuma Sales
- •
Last Author: Renato Demarchi Foresto
- •
急性腎不全
- •
尿細管障害(tubulopathy)
- •
糸球体障害(glomerulopathy)
- •
非ステロイド性抗炎症薬(NSAIDs)
- •
バンコマイシン
- •
アミノグリコシド系抗生物質
- •
シスプラチン
- •
メトトレキサート
- •
アンホテリシンB
- •
ポリミキシン
- •
テノホビル
- •
VEGF阻害薬
- •
ビスホスホネート
- •
免疫チェックポイント阻害薬
- •
高齢化
- •
慢性腎臓病(CKD)の増加
- •
糖尿病の増加
- •
腎毒性を持つ薬剤使用の増加
- •
発症機序
- •
危険因子
- •
主要薬剤
- •
臨床症候群
- •
予防・治療戦略
- •
高齢
- •
低血容量
- •
慢性腎臓病
- •
糖尿病
- •
心疾患
- •
高用量薬物
- •
低血圧
- •
複数の腎毒性薬剤の併用
- •
NSAIDs
- •
バンコマイシン
- •
アミノグリコシド
- •
シスプラチン
- •
メトトレキサート
- •
アンホテリシンB
- •
ポリミキシン
- •
テノホビル
- •
VEGF阻害薬
- •
ビスホスホネート
- •
免疫チェックポイント阻害薬
- •
プロスタグランジン阻害
- •
輸入細動脈収縮
→ GFR低下
- •
AKI発症率 5〜15%
- •
- ◦
- ◦
- ◦
リスク
用量 >4 g/day
投与期間 >14日
血中濃度上昇
- 用量 >4 g/day
- 投与期間 >14日
- 血中濃度上昇
- •
高リスク患者で最大50%のAKI
- •
AKI発症率 34%(800人以上のコホート)
- •
高用量(>500 mg/m²)でAKI
- •
発症率 最大12%
- •
KIM-1
- •
β2ミクログロブリン
- •
Clusterin
- •
Cystatin C
- 1.
早期診断
- 2.
危険因子の評価
- 3.
毒性薬剤の減量または中止
- •
血中薬物濃度モニタリング
- •
腎機能に基づく投与量調整
- •
低血容量の補正
- •
腎毒性薬剤併用の回避
- 1.
薬剤ごとの腎障害タイプを体系的に整理
- 2.
尿細管・糸球体など病態別に分類
- 3.
新規バイオマーカーの臨床応用の可能性を提示
- 4.
薬剤併用による相乗毒性(synergistic nephrotoxicity)を強調
- •
レビュー論文であり新規臨床試験データは含まれていない
- •
発症率は研究によって差がある
- •
バイオマーカーはまだ臨床標準ではない
- 1.
腎毒性薬剤のリスク評価
- 2.
抗菌薬・抗癌剤使用時の腎機能モニタリング
- 3.
腎障害の早期診断バイオマーカー開発
- 4.
薬剤投与量調整アルゴリズムの改善
- 5.
薬剤性AKI予防プログラムの設計
Awdishu L, Mehta RL. The 6R's of drug induced nephrotoxicity. BMC Nephrol. 2017 Apr 3;18(1):124. doi: 10.1186/s12882-017-0536-3. PMID: 28372552; PMCID: PMC5379580.
Title(英語)
The 6R’s of Drug Induced Nephrotoxicity
Title(日本語)
薬剤性腎毒性の6Rフレームワーク
Journal Name & Publication Year
BMC Nephrology(2017年)
First and Last Authors
- First Author: Linda Awdishu
- Last Author: Ravindra L. Mehta
First Affiliations
UC San Diego Skaggs School of Pharmacy, San Diego, USA
Abstract(要旨)
薬剤誘発性腎障害(Drug-Induced Kidney Disease: DIKD)は頻度の高い有害事象であり、患者の罹患率や医療費の増加に大きく寄与する。しかし以下の理由により、理解はまだ限定的である。
- 腎障害の定義が研究間で統一されていない
- 併存リスク因子の評価が不十分
- 長期転帰の報告が少ない
本論文では、薬剤性腎障害の管理のための**「6R framework」**を提案している。
6つの要素
- Risk(リスク評価)
- Recognition(早期認識)
- Response(対応)
- Renal support(腎サポート)
- Rehabilitation(回復・フォローアップ)
- Research(研究)
このフレームワークにより、薬剤性腎障害の予防・診断・治療を体系的に行うことが可能となる。
Background(背景)
薬剤性腎毒性は急性腎障害(AKI)や慢性腎臓病(CKD)の重要な原因である。
主なポイント
- 成人AKIの14〜26%が薬剤関連
- 小児AKIの約16%が薬剤起因
- Tenofovir使用患者では12〜22%が尿細管障害
腎毒性は以下のネフロン部位で発生する。
- 糸球体
- 尿細管
- 間質
これにより急性または慢性の腎機能障害が発生する。
Methods(方法)
本研究はレビュー論文であり、以下を目的とした概念的枠組みを提案している。
- 薬剤性腎障害のリスク評価
- 診断基準の整理
- 管理戦略の体系化
また、DIKDの臨床表現型として以下の4タイプを定義している。
- AKI(急性腎障害)
- 糸球体障害
- 尿細管障害
- 腎結石・結晶尿
さらにDIKDの時間分類
- 急性:1–7日
- 亜急性:8–90日
- 慢性:>90日
これらはKDIGOの腎障害分類に基づく。
Results(結果)
1. 6Rフレームワーク
① Risk(リスク)
リスク評価では以下を考慮
患者因子
- 高齢
- CKD
- 脱水
- 糖尿病
薬剤因子
- 高用量
- 長期投与
- 薬物相互作用
例
クラリスロマイシン+アムロジピン
→ AKI入院リスク
OR = 1.98 (95% CI 1.68–2.34)
② Recognition(認識)
多くの研究では腎毒性を
- 血清クレアチニン0.5 mg/dL増加
または
- 50%増加(24–72時間)
で定義する。
しかし以下が問題となる
- sepsisなど他原因との鑑別
- 多剤併用
- 腎機能変動
そのため標準化されたDIKD定義の必要性が強調されている。
③ Response(対応)
対応は以下に依存
- 腎障害のタイプ
- 重症度
- 治療必要性
例
Type A(用量依存毒性)
- 用量減量
- TDM(Therapeutic Drug Monitoring)
Type B(特異反応)
- 薬剤中止
例
Vancomycin腎毒性
- 発生率 5–43%
- trough >15 ng/mLでリスク増加
OR 2.67
④ Renal Support(腎サポート)
腎代替療法は
目的
- 腎機能補助
- 薬物除去
例
- vancomycin
- aminoglycoside
透析による薬物除去は
- 分子量
- 蛋白結合
- 分布容積
などに依存する。
⑤ Rehabilitation(回復)
多くの薬剤性AKIは
- 非乏尿性
- 薬剤中止で回復
しかし例外もある。
例
cisplatin
- GFR低下 → 回復
- 尿細管障害 → 持続する場合あり
重要事項
- AKI外来フォロー
- 再曝露防止
- 副作用報告(FDA MedWatch)
⑥ Research(研究)
DIKD研究の課題
- 定義の不統一
- 因果関係評価の困難
- 長期転帰データ不足
将来の研究領域
- バイオマーカー
- 遺伝的感受性
- EMRベースの監視システム
電子医療記録による薬剤性AKIの早期検出が有望とされている。
Discussion(考察)
薬剤性腎障害は
- 多因子
- 多剤併用
- 基礎疾患
が絡み合うため診断が難しい。
6Rフレームワークは
- 予防
- 早期診断
- 適切な治療
を体系化した臨床ツールとして提案されている。
特に
- EMR監視
- TDM
- 腎機能モニタリング
の重要性が強調されている。
Novelty compared to previous studies(新規性)
本研究の新規性
- 薬剤性腎障害管理の6Rモデル提案
- DIKDの4つの表現型定義
- 電子医療記録による監視システムの提案
- リスク評価から研究までを包括した管理体系
これにより臨床・研究双方で標準化が可能となる。
Limitations(限界)
- 実験研究ではなくレビュー
- 定量的解析が少ない
- 因果関係評価ツールは未確立
Potential Applications(応用可能性)
臨床応用
- ICUにおける薬剤性AKI予防
- 抗菌薬治療の安全管理
- 電子カルテ警告システム
- 腎毒性リスクスコア開発
研究応用
- バイオマーカー開発
- AIによる腎毒性予測
- 薬物遺伝学研究