糖尿病
|病態と作用機序
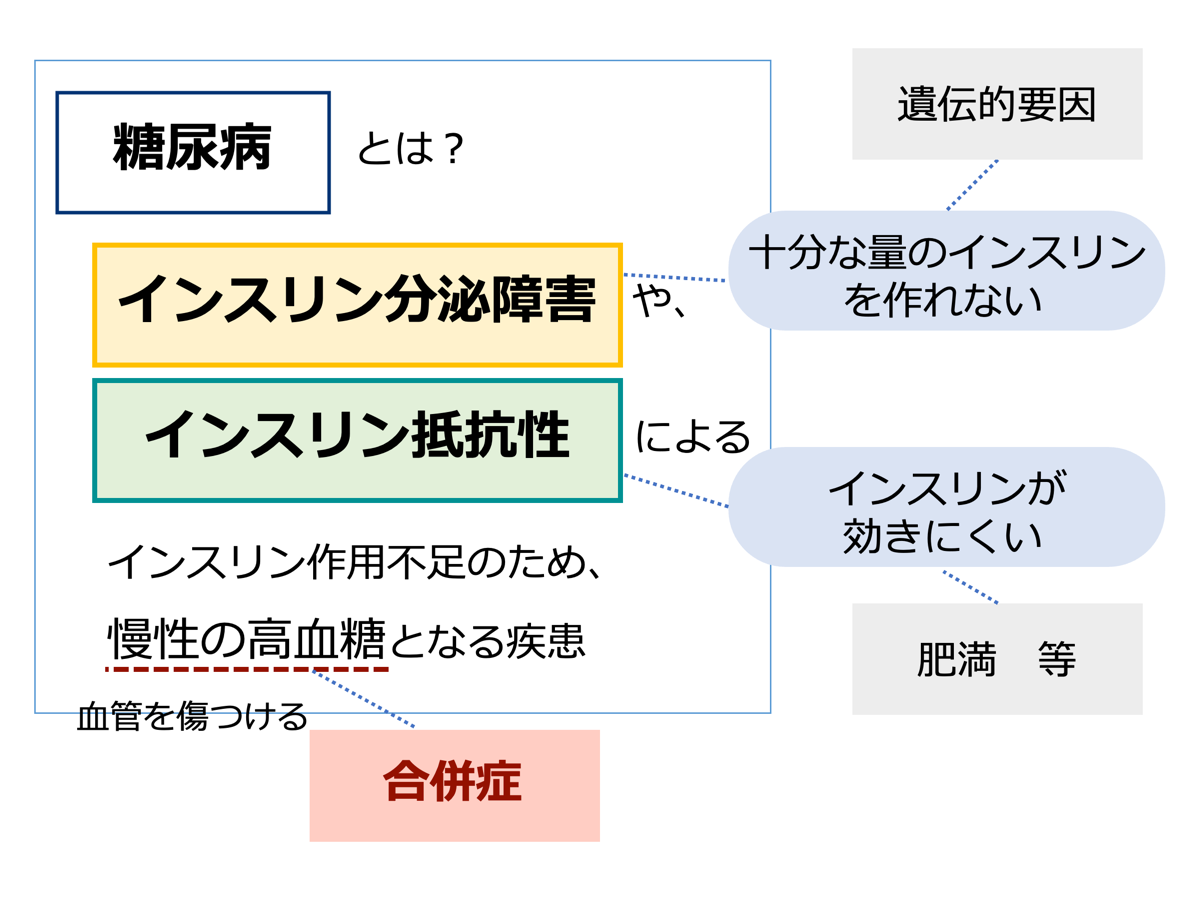
糖尿病(Diabetes mellitus)とは、インスリンの分泌不足や作用不全によって慢性的に高血糖をきたす代謝疾患の総称です。
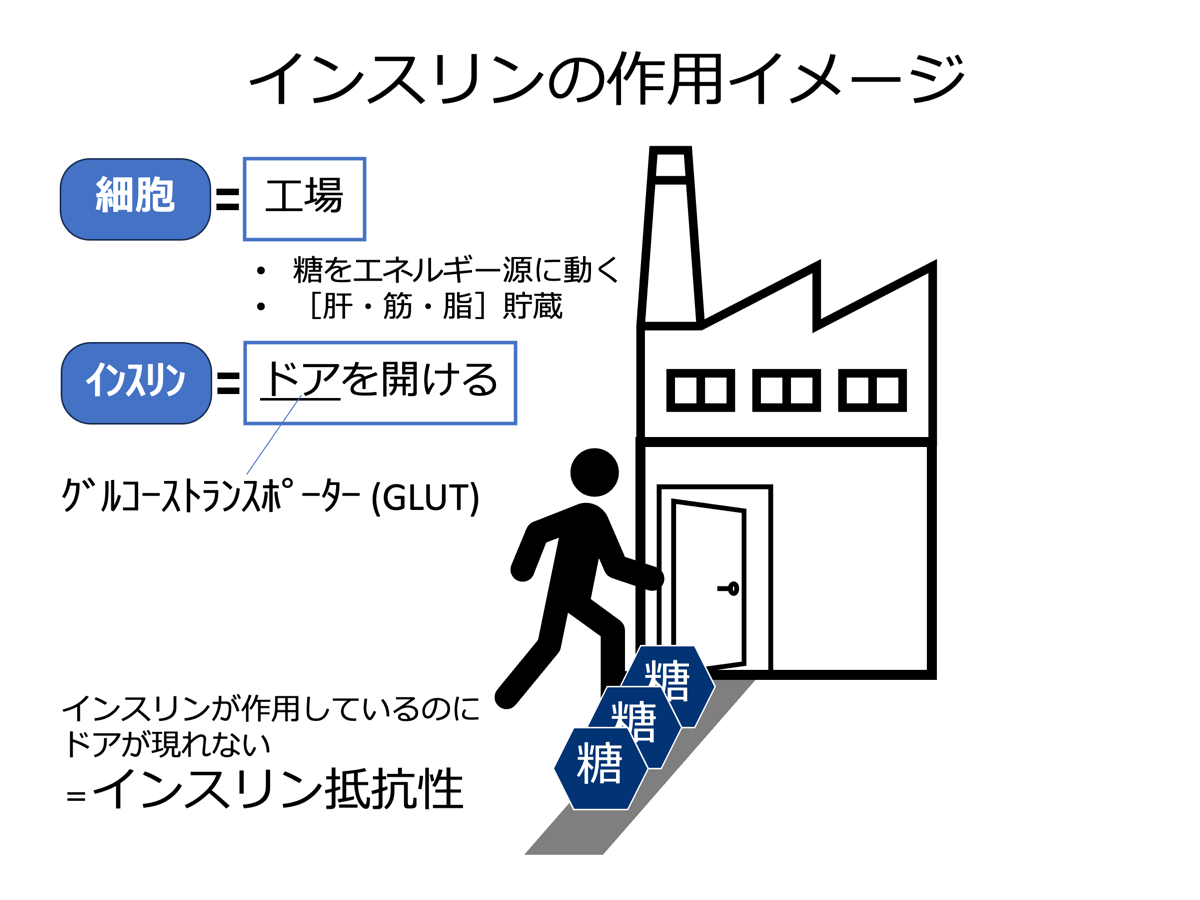
インスリンとは:
細胞を燃やすエネルギーである糖を、細胞に入れるためにドアを開ける役割
- インスリンの作用が不足(分泌障害や抵抗性)すると、
- 細胞はエネルギーが不足する
- 血中に糖が過剰にあふれる
- 急性の影響
- 慢性の影響
脱水
ケトアシドーシス
ブドウ糖の代わりに脂肪をエネルギー源として使った結果、ケトン体が蓄積する
血管を傷つける
余分な糖がタンパク質などと結合(糖化)する→炎症や酸化ストレスの原因となる→血管を傷つける
|薬物治療
治療目標
ライフスタイル
- 食事療法
- エネルギー摂取量の適正化(標準体重×25 kcal/日など)
- 主食・主菜・副菜のバランス(糖質制限ではなく食事総量のコントロール)
- 食事タイミングと間食の管理
- 運動療法
- 有酸素運動:週150 分以上(ウォーキング、サイクリングなど)
- レジスタンストレーニング:週2回程度筋力トレーニング
- 日常生活活動の増加(階段利用、家事動作の活用)
薬物療法
- インスリン分泌促進系
- DPP-4 阻害薬、GLP-1 受容体作動薬、SU薬、グリニド薬 など
- インスリン感受性改善系
- ビグアナイド薬(メトホルミン)、チアゾリジン薬(ピオグリタゾン)
- 糖吸収・排泄調節系
- α-グルコシダーゼ阻害薬、SGLT2 阻害薬 など
- インスリン療法
- 持効型/超速効型インスリン、混合製剤、CSII(持続皮下インスリン注入)
→ 患者さんの年齢、腎機能、低血糖リスク、合併症状況に応じて、単剤開始から多剤併用へステップアップ
セルフケア
- SMBG の活用:血糖値のパターンを把握し、治療効果や低血糖リスクを評価
- インスリン療法
- セルフケア教育:食事内容の記録、運動記録、薬剤服用の遵守、低血糖対応
- フットケア・歯科管理:末梢神経障害や歯周病予防
合併症の予防・管理
- 急性合併症:低血糖、糖尿病性ケトアシドーシス
- 慢性合併症
- 微小血管障害:糖尿病性網膜症、腎症、神経障害
- 大血管障害:虚血性心疾患、脳血管障害、下肢血管障害
- 定期的な眼科・腎機能・神経学的フォロー、足病変チェック
治療の個別化と多職種連携
- 個別化:患者さんの価値観、ライフスタイル、コンプライアンス、合併症リスクに最適化
- 多職種アプローチ:医師、看護師、薬剤師、栄養士、保健師、理学療法士などがチームで支援
血糖値だけではなく、全体を見る
食事療法・運動療法・薬物療法の3本柱に加え、合併症も一緒に治療・予防することが重要であるため、禁煙・歯周病治療を加えて5本柱とされている。
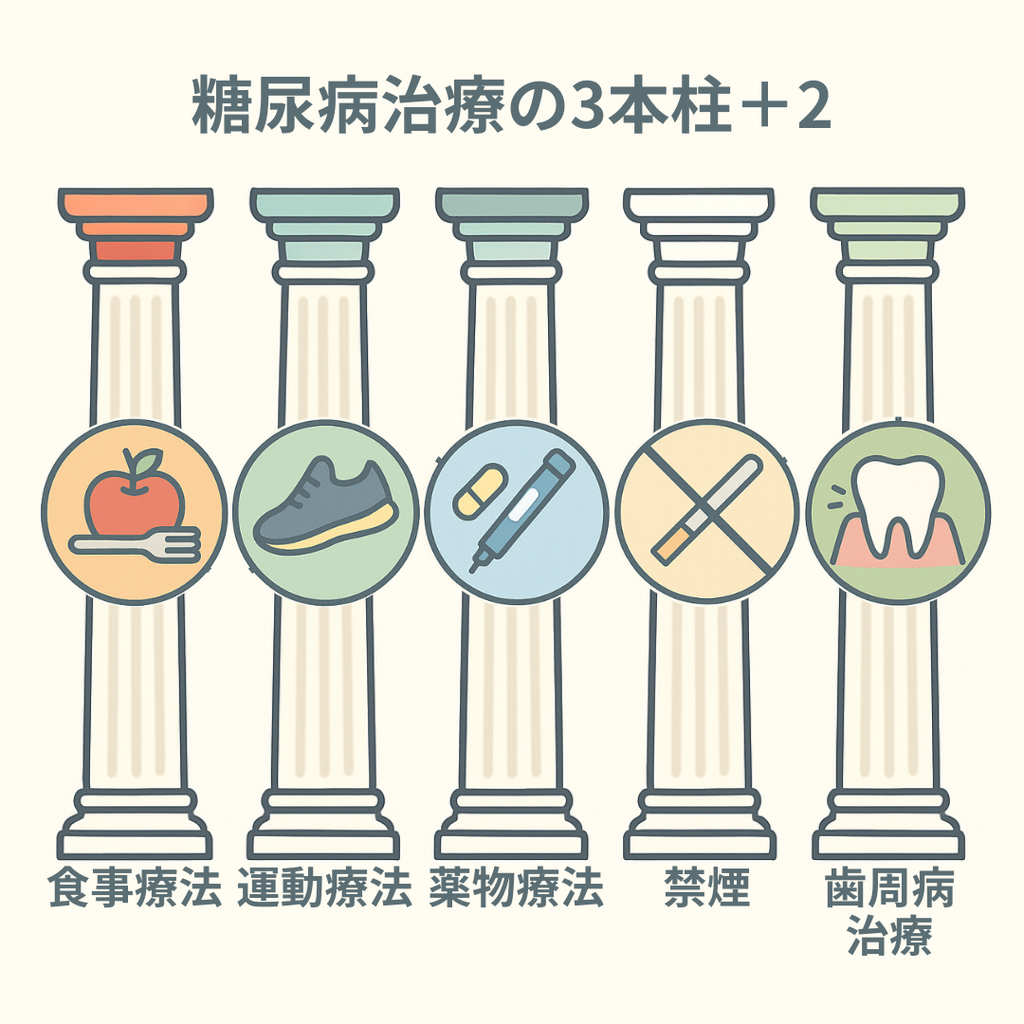
治療目標
- 糖尿病がない人と変わらない生活の質 (QOL, quality of life) と寿命を実現すること
|治療薬一覧
|治療目標/血糖コントロール HbA1c
成人糖尿病の血糖コントロール目標 熊本宣言 ・血糖正常化を目指す際の目標:6.0未満 ・合併症予防のための目標:7.0未満 ・治療強化が困難な際の目標:8.0未満 https://www.jds.or.jp/modules/important/index.php?content_id=42

高齢者糖尿病の血糖コントロール目標 https://www.jds.or.jp/modules/important/index.php?content_id=66
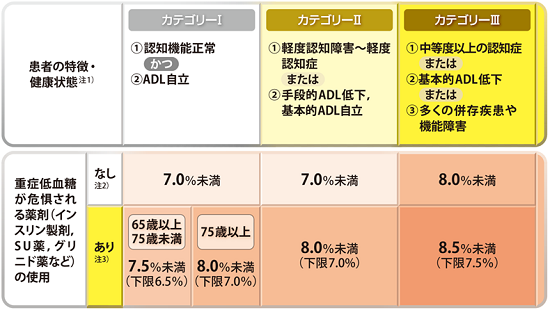
|薬物治療中の注意点
薬物治療中に注意しておきたいこと
|リハ栄養と糖尿病治療薬
生活面に対する各薬効群の影響まとめ
糖尿病とサルコペニア
糖尿病とサルコペニアは悪循環を形成する(疾患自体)
メトホルミン
効果:AMPK活性化や抗炎症作用を通じ、筋細胞の老化(セネセンス)抑制、筋炎症の軽減、筋線維の萎縮防止に寄与
(RCT)筋量維持
Petrocelli JJ, McKenzie AI, de Hart NMMP, Reidy PT, Mahmassani ZS, Keeble AR, Kaput KL, Wahl MP, Rondina MT, Marcus RL, Welt CK, Holland WL, Funai K, Fry CS, Drummond MJ. Disuse-induced muscle fibrosis, cellular senescence, and senescence-associated secretory phenotype in older adults are alleviated during re-ambulation with metformin pre-treatment. Aging Cell. 2023 Nov;22(11):e13936. doi: 10.1111/acel.13936. Epub 2023 Jul 24. PMID: 37486024; PMCID: PMC10652302.
研究デザイン(PICO)
- P(対象):BMI<30、60歳以上の健康な男女20名
- I(介入):メトホルミン(標準用量)を2週間の投与+5日間のベッドレスト開始前に継続
- C(比較):プラセボ投与群
- O(評価項目):
- 筋線維のサイズ(萎縮度)
- 筋組織の炎症関連遺伝子発現プロファイル
- 筋間質(ECM)中のコラーゲン沈着量
- 筋組織および前駆細胞(FAPs)の細胞老化(セネセンス)マーカー/SASP(senescence-associated secretory phenotype)
主要な結果
- 筋線維萎縮の軽減
- ベッドレスト中のタイプI筋線維の萎縮がメトホルミン群で有意に小さかった。
- 炎症プロファイルの改善
- ベッドレスト期・回復期ともに、メトホルミン群でプロ炎症性遺伝子の発現が低下。
- ECMリモデリングの改善
- 回復期の筋組織におけるコラーゲン沈着量がプラセボ群よりも低減。
- 細胞老化およびSASPの抑制
- 筋組織中のセネセンスマーカーおよびSASP関連因子が低く、
- 筋線維周囲の線維芽細胞(FAPs)では、老化マーカーの減少と線維化型(myofibroblast-like)への分化傾向の低下を認めた。
結論
メトホルミンを再歩行前に投与することで、加齢による不動期間(ベッドレスト)後の筋回復過程において
- 筋萎縮・炎症・細胞老化の抑制
- ECM(特にコラーゲン)過剰沈着の軽減
が見られ、筋組織のリモデリングが改善される可能性が示された。
臨床的示唆
高齢者の不動時(手術後や長期臥床など)にメトホルミンをプレメディケーションとして用いることで、筋機能の維持・回復を助ける新たな戦略となり得る。
(RCT)4 m歩行速度の改善効果は認められなかった
Metformin and physical performance in older people with probable sarcopenia and physical prefrailty or frailty in England (MET-PREVENT): a double-blind, randomised, placebo-controlled trial
Witham, Miles D et al.
The Lancet Healthy Longevity, Volume 6, Issue 3, 100695
P (Population/対象)
- 年齢 ≥ 65歳の高齢者(平均80.4歳、SD 5.7)
- 4 m歩行速度 < 0.8 m/s かつ
- 握力低下(女性<16 kg、男性<27 kg)
- または 5回立ち上がり試験 > 15 秒(あるいは完遂不能)
- Probable sarcopenia かつ physical prefrailty または frailty
I (Intervention/介入)
- 経口メトホルミン 500 mg を1日3回、4ヶ月間投与
- n = 36
C (Comparison/比較)
- マッチングプラセボを同量・同頻度で投与
- n = 36
O (Outcome/評価項目)
- 主要評価項目:4ヶ月後の4 m歩行速度(調整後群間差)
- メトホルミン群:0.57 m/s (SD 0.19)
- プラセボ群:0.58 m/s (SD 0.24)
- 差 0.001 m/s(95% CI –0.06~0.06)、p = 0.96 → 有意差なし
- 安全性評価:
- 有害事象(メト群108件/35例、プラ群77件/33例)
- 入院(メト群12例〔34%〕、プラ群3例〔8%〕)
- 死亡:メト群1例(関連性なしと判断)
解釈
- メトホルミン投与は、4 m歩行速度を改善せず、むしろ忍容性に課題があることが示された。
- 高齢サルコペニア・フレイル疑い者への適用は慎重を要する。
(in vitro、動物モデル)骨・筋・関節への影響
Song Y, Wu Z, Zhao P. The Function of Metformin in Aging-Related Musculoskeletal Disorders. Front Pharmacol. 2022 Mar 8;13:865524. doi: 10.3389/fphar.2022.865524. PMID: 35392559; PMCID: PMC8982084.
PECO 構造による要約
- P (Population):
- 高齢者や加齢モデル(老化に伴う骨粗鬆症、サルコペニア、変形性関節症、脆弱性を呈するマウスや線虫など)PMC
- E (Exposure/Intervention):
- C (Comparison):
- 無投与(コントロール)、プラセボ、または従来治療(運動のみ、標準管理のみなど)OUCI
- O (Outcomes):
- 骨ホメオスタシスの改善
- CV-MSCs(ヒト絨毛間葉系幹細胞)において、アルカリホスファターゼ、RUNX2、オステオポンチンなどの骨芽細胞マーカー mRNA 発現上昇と石灰化促進が認められた。J-STAGE
- 筋細胞保護・機能維持
- 運動誘発性の筋障害を軽減し、ミトコンドリア機能や筋適応を支える作用が示唆された(運動パフォーマンス自体は向上しないものの、筋細胞障害は抑制)。OUCI
- 関節軟骨保護・炎症抑制
- AMPK 経路活性化を介し、変形性関節症モデルマウス(および一部霊長類モデル)で関節軟骨の退行を遅延させ、痛み感受性を低減。セラノスティクス
- 寿命延長・全死因死亡減少
- C. elegans やマウスで寿命延長効果、さらにヒトでは観察研究において全死因死亡率の低下が報告されている。セラノスティクス
批判的吟味
- エビデンスの質と対象
- 骨・筋・関節への作用機序は in vitro や動物モデルで精緻に検討されている一方、ヒトのランダム化試験(RCT)は乏しく、多くは観察研究やレトロスペクティブ解析に依存している。
- メトホルミン投与量や投与期間、被験者の選択基準(糖尿病合併の有無、高齢度など)が研究間で大きく異なり、結果の一般化には注意が必要である。
- 用量反応関係と安全性
- in vitro 研究では 0.05 mM 前後のメトホルミンが用いられるが、これはヒト血中濃度と一致しない可能性がある。動物モデルからヒトへの換算にはさらなる検証が必要。
- 長期投与による微小な副作用(ビタミンB₁₂欠乏、乳酸アシドーシスリスクなど)も、特に高齢者では慎重なモニタリングが求められる。
- 臨床的意義とアウトカム
- 筋機能向上や骨折リスク低下、関節痛緩和など、臨床的に「意味のある」アウトカムを評価した RCT の実施が遅れている。サルコペニアの筋力測定(握力、歩行速度など)や骨密度、関節機能スコアを用いた厳格な試験設計が望まれる。
- 観察研究で示唆された全死因死亡率低下も、交絡因子(ライフスタイル、併用薬など)の影響を完全に除外できていない。
- 総括と今後の展望
- メトホルミンは長期にわたる安全性プロファイルが確立されており、老化関連疾患へのリパーパスが有望である。
- しかし、翻訳研究のギャップを埋めるため、用量設定・被験者選択・エンドポイントの明確化を行った多施設共同 RCT の実行が急務である。
以上より、本レビューはメトホルミンの多面的な抗老化作用を示す有力な基礎データを提供する一方で、ヒトへの適用にはさらなる臨床試験および長期フォローアップが不可欠であることが示唆される。
スルホニル尿素薬/グリニド薬(SU薬・速効型インスリン分泌促進薬)
影響:動物実験および一部臨床で筋萎縮の促進が示唆されており、サルコペニア悪化リスクがある。
SGLT2 阻害薬
影響:糖尿排泄による総体重・脂肪量減少の一環で筋量も減少するリスクがある。
抗炎症作用
肥満症
糖尿病治療薬とサルコペニア
血糖降下薬がサルコペニアに及ぼす影響
|栄養療法と高齢者糖尿病
出典を確認
- 予防
CQ17a:予防に食事・栄養は有用か? (サルコペニア・フレイルに関する栄養管理ガイドライン2025)
- 高齢者を含む2型糖尿病患者に対するロイシン・ビタミンD・ホエイたんぱく質などを含む複合栄養介入によるサルコペニアならびにフレイルの予防効果について、今のところ研究が乏しく十分なエビデンスはないものの効果は期待でき、行うことを提案する。 (推奨の強さ:弱, エビデンスの確実性:C)
- 高齢者を含む2型糖尿病患者に対するアミノ酸・たんぱく質摂取または栄養指導(アミノ酸・たんぱく質摂取の最適量の維持または充足を図る指導)とレジスタンス運動との併用によるサルコペニアの予防効果について、必ずしも介入研究の結果は一致していないものの効果は期待でき、行うことを提案する。
(推奨の強さ: 弱、エビデンスの確実性: B)
- 高齢者を含む2型糖尿病患者に対する栄養指導(たんぱく質摂取を含む最適な栄養状態を維持するための栄養指導)と運動(レジスタンス運動または身体機能の強化)の併用によるフレイルの予防効果については、なお研究が乏しく十分なエビデンスはないものの効果は期待でき、行うことを提案する。
(推奨の強さ: 弱、エビデンスの確実性: C)
- 食事療法
CQ17b : 治療に食事・栄養療法は有用か? (サルコペニア・フレイルに関する栄養管理ガイドライン2025)
- サルコペニアまたはフレイルを合併した2型糖尿病患者を対象とした食事または栄養の単独療法の治療効果に関してはエビデンスにつながる介入研究は少なかったが、最適な栄養状態の維持を目的とした栄養指導とレジスタンス運動との併用により身体機能が改善する可能性があり、行うことを推奨する。 (推奨の強さ: 強、エビデンスの確実性: B)
- エネルギー
VII-3 高齢者糖尿病の治療開始時のエネルギー指示量を決める際にはどのような点に注意すべきか? (高齢者糖尿病診療ガイドライン2023)
【ポイント】
- 「総エネルギー摂取量の目安」は、年齢を考慮に入れた「目標体重」と「身体活動レベルと病態によるエネルギー係数」から算出する。
- 高齢者においては「目標体重」を一律に定めるのではなく、現体重に基づき、年齢や臓器障害など、患者の属性や代謝状態を評価しつつ、目安となる体重を段階的に再設定するなど柔軟に配慮してよい。
- 目標体重・・・算出に用いるBMIは年齢ごと
- 65歳未満: [身長(m)]× 22
- 65歳から 74歳 : [身長(m)]× 22~25
- 75歳以上 : [身長(m)]× 22~25 で算出する
ただし、75歳以上は、現体重に基づき、フレイル、(基本的)ADL 低下、併存疾患、体組成、身長の短縮、摂食状況や代謝状態の評価を踏まえ、適宜判断
- 身体活動レベルと病態によるエネルギー係数
- 軽い労作(大部分が座位の静的活動):25~30 kcal/kg 目標体重
- 普通の労作(座位中心だが通勤・家事、軽い運動を含む):30~35 kcal/kg 目標体重
- 重い労作(力仕事、活発な運動習慣がある):35~ kcal/kg 目標体重
ただし、高齢者のフレイル予防では、身体活動レベルより大きい「エネルギー係数」を設定できる
(高齢者糖尿病診療ガイドライン2023)
- タンパク質摂取量
VII-7 フレイル・サルコペニアの予防を目的とした高齢者糖尿病のタンパク質摂取量を決める際にはどのような点に注意すべきか? (高齢者糖尿病診療ガイドライン2023)
【ポイント】
- 高齢者糖尿病ではタンパク質の摂取不足によるフレイルやサルコペニアの発症に注意する。
- 高齢者のフレイル・サルコペニアの予防のためには十分なタンパク質を摂る。
欧州臨床栄養代謝学会(ESPEN)のexpert groupの推奨
- フレイル・サルコペニア対策のためのタンパク質摂取量
- 健康な高齢者:1.0~1.2g/kg 実体重/日以上
- 低栄養または低栄養のリスクがある高齢者:1.2~1.5g/kg 実体重/日
- ESPENガイドライン(2018)
- 高齢者でのタンパク質摂取量:1.0g/kg実体重/日以上
- 栄養状態、身体活動レベル、併存疾患の状態、忍容性に応じて個別に設定すべき
(高齢者糖尿病診療ガイドライン2023)
CQ17c : 食事・栄養療法は死亡、入院、ADL低下などの転帰不良を改善させるか? (サルコペニア・フレイルに関する栄養管理ガイドライン2025)
- 食事・栄養療法の糖尿病に伴うサルコペニアならびにフレイルに対する転帰不良への効果に関するエビデンスに資する報告はないが、高齢2型糖尿病患者(75歳以上)に対する十分なたんぱく質摂取(1.15 g/kg/日以上)が死亡を抑制する可能性があり、行うことを提案する。
(推奨の強さ: 弱、エビデンスの確実性: C)
|併存疾患
- 腎臓
- 一般社団法人 日本透析医学会:「透析患者の糖尿病治療ガイド2025」、2025年6月1日、医学図書出版.https://igakutosho.co.jp/collections/book/products/ur_059
- 一般社団法人 日本透析医学会:「血液透析患者の糖尿病治療ガイド 2012」、透析会誌、46、311〜357 (2013).