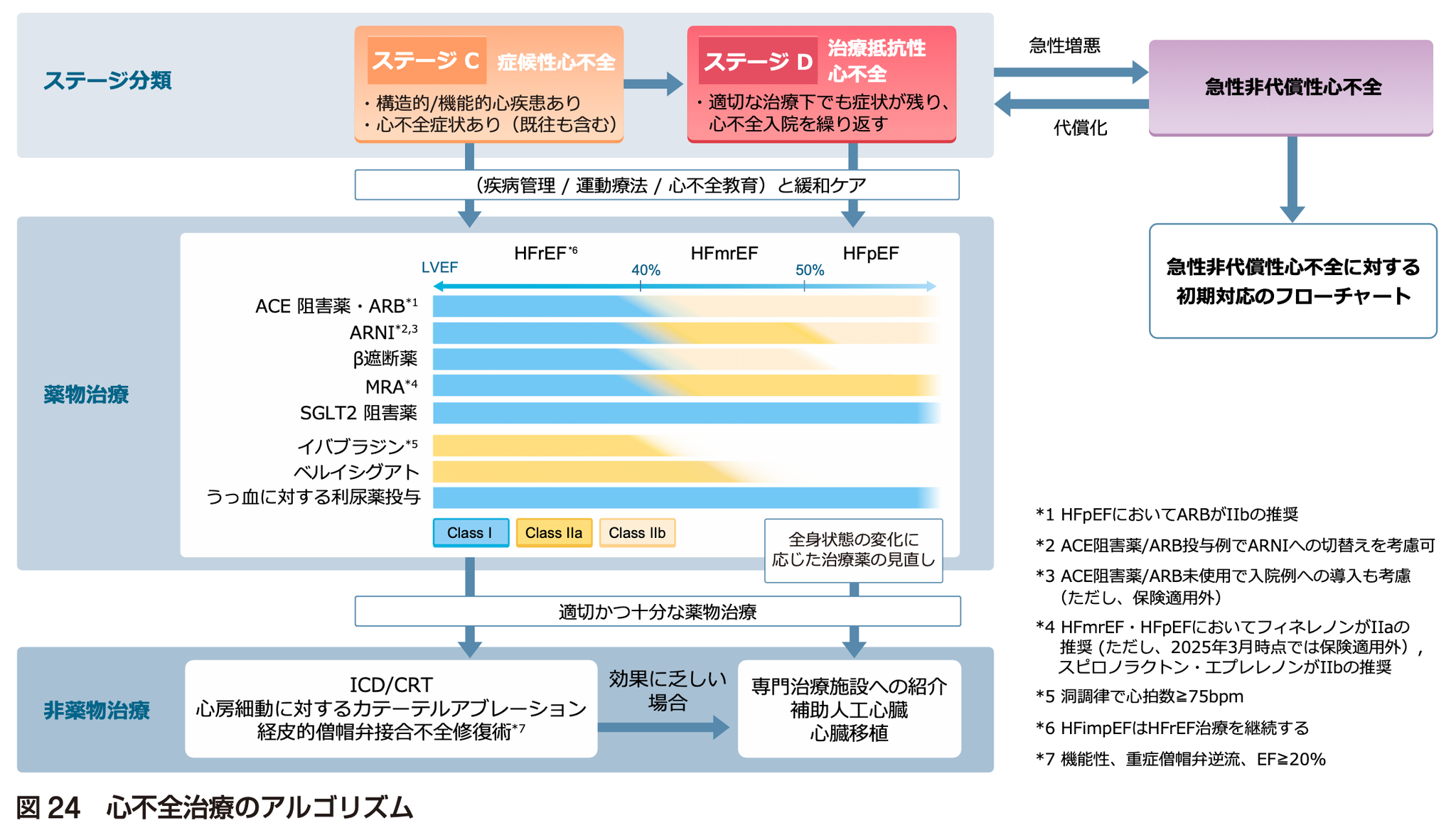
慢性心不全
慢性心不全治療に用いられる薬
ガイドラインに基づいた心不全治療(Guideline-Directed Medical Therapy)の実践
症状の緩和・QOL(生活の質)の向上
- うっ血性症状(呼吸苦、浮腫など)を軽減し、日常生活をしやすくする。
- 運動耐容能を改善し、活動量を増やすことで体力低下を予防。
心機能の保護・リモデリング抑制
- 心不全では交感神経・RAAS(レニン‐アンジオテンシン‐アルドステロン系)が過剰に活性化され、心筋の線維化や肥大(リモデリング)が進行する。これを薬剤で遅延または抑制し、長期的な心機能低下を防止する。
- 心不全の進行を抑え、頻回の入退院を減らす。
予後改善(死亡率低下)
- 特に左室駆出率(LVEF)低下例では、心臓突然死や心不全死を減らすことが薬物選択の大きな指針となる。
- ガイドラインで示される治療薬を適切に組み合わせることで、入院リスクや全死亡率を低下させる。
心不全の 4pillar
構成
- ARNI(or ACE阻害薬 / ARB)
- β遮断薬
- MRA
- SGLT2阻害薬
コンセプト
- 発症・進行の異なる病態を同時に叩く
- 低用量でもOK → とにかく早期に4剤そろえる
- 目的は明確
👉 死亡↓・心不全入院↓
ARNI(or ACE阻害薬 / ARB)
- ACE阻害薬
- ARB(アンジオテンシンⅡ受容体拮抗薬)
- ARNI(アンジオテンシン受容体ネプリライシン阻害薬)
- RAAS抑制・・・ACE阻害薬、ARB、ARNIのバルサルタン部分
- 血管拡張・ナトリウム利尿を促進し、前負荷・後負荷を軽減。
- 心筋リモデリング抑制による予後改善。
- ブラジキニン増加・・ACE阻害薬のみ
- さらに血管拡張・抗線維化作用
- ネプリライシン阻害(サクビトリル成分)
- ナトリウム利尿ペプチド(ANP、BNPなど)の分解を抑制し、利尿・血管拡張・抗線維化作用を増強
- β₁受容体遮断:
- 交感神経活性を抑えて心拍数・心収縮力を適度に低下させ、心筋酸素消費を減らす。
- リモデリング抑制:
- 長期的には心筋リモデリング(肥大・線維化)を抑え、心機能悪化を遅延。
MRA(ミネラルコルチコイド受容体拮抗薬)
- アルドステロン作用をブロックし、ナトリウム利尿・線維化抑制を介して心リモデリングをさらに防止。
- 再入院・死亡リスクを減少。
SGLT2阻害薬(ナトリウム・グルコース共輸送体2阻害薬)
- 腎臓でのナトリウム・グルコース再吸収を抑制し、利尿効果で前負荷を軽減。
- 心筋保護作用も示されており、心不全入院・死亡を抑制。
併用薬
- 心拍数を低下させ、心臓を保護する
- 心不全患者の心不全入院リスク軽減
- NO非依存的にsGCを直接刺激し、cGMP産生を増加させ、平滑筋弛緩や血管拡張をもたらす
SGLT2阻害薬
うっ血改善
ループ利尿薬
- 体液貯留による肺うっ血・浮腫を速やかに改善し、症状の緩和とQOL維持に寄与。
- 前負荷の即時軽減が中心で、予後改善薬ではなく症状コントロール用。
強心薬
ジギタリス製剤
予後改善薬・・・できるだけ早く導入し、徐々に増量し、最大耐用量を継続
→副作用は早期に対応する
| 薬理作用 | 主な効果 | 投与ポイント |
| RA系抑制(ACEi/ARB) | 血管拡張・線維化抑制 | 血圧低下に注意、空咳(ACEi)、腎機能・電解質モニター |
| ARNI | 強化ナトリウム利尿・血管拡張 | ARB切替後開始、頻脈性血行動態確認、6時間間隔投与 |
| β遮断 | 心拍数・収縮力抑制、リモデリング抑制 | 低用量から徐増、HR・BP・AV伝導モニター |
| MRA | 線維化抑制・利尿 | 高K血症に注意、腎機能・Kモニター |
| SGLT2阻害 | 心腎保護・利尿 | 尿路感染注意、脱水リスク回避、eGFR下限確認 |
| イバブラジン | 選択的心拍数低下 | 安静HR≥70 bpm、β遮断十分投与下で適用 |
| ヒドララジン+硝酸薬 | 血管拡張(前負荷・後負荷軽減) | 頻回投与、頭痛や低血圧に注意 |
- 血圧低下・徐脈
- 対策:低用量漸増、バイタルモニター、降圧薬併用の見直し。
- 腎機能悪化・高K血症(RA系抑制/MRA)
- 対策:BUN/Cre・電解質定期チェック、利尿薬調整。
- 尿路・性器感染症(SGLT2阻害)
- 対策:排尿衛生指導、脱水予防の水分摂取指導。
- ナトリウム利尿過剰/脱水
- 対策:体重・血圧・電解質モニター、抗利尿薬調整。
- 空咳(ACE阻害)
- 対策:ARBまたはARNIへの切替検討。
- 頭痛・顔紅潮(ヒドララジン)
- 対策:服用タイミング調整(就寝前投与など)。
- 洞房結節機能低下(イバブラジン)
- 対策:投与基準厳守(安静HR≥70 bpm)、心電図モニター。
ポイント:
ガイドライン
📚 4. 各種レビュー/ガイドライン
- JACCやAHA/ACC/HFSA、CCS(カナダ心不全学会)などのガイドラインは、「入院中または診断早期に、4本柱(RAASi/ARNI・β遮断薬・MRA・SGLT2i)を迅速に導入・最適化すべき」と明記。
- CCSガイドは「診断後3〜6ヶ月以内に主要4剤を全て開始し最適化すべき」としていますverywellhealth.com+4acc.org+4uscjournal.com+4。
JACC https://pubmed.ncbi.nlm.nih.gov/30922510/
Title(英語・日本語)
Target Dose Versus Maximum Tolerated Dose in Heart Failure: Time to Calibrate and Define Actionable Goals
心不全における目標用量と最大耐用量:調整と実行可能な目標の定義が必要な時
Journal Name & Publication Year(雑誌名・出版年)
JACC: Heart Failure, 2019年
First and Last Authors(第一著者と最終著者)
First Author: Biykem Bozkurt
Last Author: Biykem Bozkurt
First Affiliations(第一所属機関)
Section of Cardiology, Michael E. DeBakey VA Medical Center, Baylor College of Medicine, Houston, Texas, USA
Abstract(要旨)
本論文は、心不全治療における目標用量(target dose)と最大耐用量(maximum tolerated dose)のギャップについて論じている。臨床試験で推奨される目標用量は、多くの患者で達成可能とされるが、現実の臨床では達成率が低い。副作用や医師の判断、システム上の制約などが原因とされる。CHAMP-HFレジストリに基づくデータを引用し、ガイドラインに基づく治療(GDMT)の達成状況と血圧・心拍数との関連も検討している。
Background(背景)
ACE阻害薬やβ遮断薬の最大用量の有効性は長年の研究で証明されているが、実臨床では十分な投与が行われていない。多くの理由で目標用量への到達が困難であり、実際には最大耐用量での治療が現実的であることが多い。
Methods(方法)
本稿は編集論説であり、Peri-OkonnyらのCHAMP-HFレジストリに基づく研究結果にコメントしている。レジストリデータにより、患者の血圧や心拍数、治療薬の使用率、目標用量達成率などを分析。
Results(結果)
- ACEI/ARBの目標用量到達率:10.8%
- β遮断薬:18.7%
- ARNi:2.0%
- SBPが110 mmHg以上の患者でも目標用量到達率は10%以下
- SBPやHRが目標用量達成の大きな障害ではないことが示唆された
Discussion(考察)
心不全患者への標準治療の最適化は十分でない。目標用量の達成は重要であるが、個々の患者の耐用性を記録し、達成不可能な場合には最大耐用量を記録することも重要なパフォーマンス指標となる。
Novelty compared to previous studies(先行研究との新規性)
目標用量と実際の使用量の乖離に注目し、最大耐用量という現実的な視点からパフォーマンス指標の改善を提案している点が新しい。
Limitations(限界)
- データの限界(後続の血圧測定や治療変更の記録なし)
- 登録患者の人種や医療環境の偏り
- 全患者に一般化できない可能性あり
Potential Applications(応用可能性)
- 医療現場でのGDMTの導入・最適化
- 患者個別の最大耐用量の記録による治療目標設定の明確化
- ガイドラインの現実的適用とパフォーマンス評価基準の改善
目標用量の到達を妨げている主な障壁は、以下のように論文内で具体的に述べられています:
- 患者側の要因
- 薬物に対する不耐性(intolerance)
- 副作用(side effects)
- *低血圧(SBP <110 mmHg)や徐脈(HR <60 bpm)**といった生理的制限(ただし、これらは大きな障害とは限らないと報告)
- 医療提供者側の要因
- 医師の回避傾向(provider aversion)
- 治療慣性(clinical inertia)=治療の変更や増量を避ける傾向
- 医療システム側の要因
- 医療記録やコーディングの不備(禁忌や不耐性の十分な記録がない)
- データ不足やコスト制限
- 試験と実臨床の違い
- 臨床試験に含まれない高リスクや末期の患者が現実の診療には多く含まれ、試験データとの乖離が生じている
これらの複合的な要因により、目標用量への到達率は依然として低く、最大耐用量の明確化と記録が重要な代替戦略とされています。
「最大耐容量(maximally tolerated dose)」まで増量することで、死亡率や心不全による入院を減少させる効果がある
副作用などの問題がある場合、忍容性が許す限り最大耐容量まで増量する
ACEi/ARB/ARNI
ATRAS 試験 https://pubmed.ncbi.nlm.nih.gov/10587334/
🔍 研究の目的
ACE阻害薬は慢性心不全(CHF)に有効とされるが、臨床現場では低用量で使用されることが多い。この研究では、低用量と高用量のリシノプリル(ACE阻害薬)による有効性の差を検討した。
🧪 研究デザイン
- 試験名:ATLAS(Assessment of Treatment with Lisinopril And Survival)
- デザイン:多施設・無作為化・二重盲検比較試験
- 対象者:心不全(NYHAクラスII~IV)、EF≦30%の患者 3,164例
- 介入:
- 低用量群:リシノプリル 2.5–5.0 mg/日(n=1596)
- 高用量群:リシノプリル 32.5–35 mg/日(n=1568)
- 追跡期間:平均 39〜58か月
- 併用療法:心不全の標準治療を継続
📊 主な結果
| 指標 | 高用量 vs 低用量 | 結果 |
| 全死亡率 | 8%低下 | 有意差なし(P=0.128) |
| 死亡 or いかなる理由による入院 | 12%低下 | 有意差あり(P=0.002) |
| 心不全による入院 | 24%減少 | 有意差あり(P=0.002) |
| 副作用 | めまい、腎機能障害は高用量群でやや多い | しかし中止率に差なし |
✅ 結論
- 高用量リシノプリルは低用量と比較して、心不全による入院の抑制や複合アウトカムにおいて優れている。
- 死亡率の低下は統計的には有意でなかったが臨床的意義がある可能性あり。
- 低用量は、忍容性の問題がある場合に限り選択されるべき。
- 中間用量と高用量との間の効果差は小さいと考えられる。
🩺 臨床的インプリケーション
心不全治療において、可能であれば最大耐量までACE阻害薬を漸増すべきという実践的な指針を支持するエビデンス。
PARALLEL-HF 試験 https://www.jstage.jst.go.jp/article/circj/88/1/88_CJ-23-0174/_article
🧪【研究の背景と目的】
- PARALLEL-HF試験は、日本人の**慢性心不全・左室駆出率低下(HFrEF)**患者において、サクビトリル/バルサルタン(ARNI)とエナラプリルを比較した初の第III相試験。
- この**オープンラベル延長試験(OLE)**では、ARNIの長期的な安全性と忍容性を評価。
👥【対象と方法】
- 対象者:PARALLEL-HFの試験終了後に登録された150名のHFrEF患者
- ARNIコア群:初回試験でもARNIを使用した群
- エナラプリル→ARNI群:初回試験でエナラプリル→延長試験でARNIに切替え
- 投与量:サクビトリル/バルサルタン 50または100mg 1日2回 → 8週目までに目標200mg 1日2回へ漸増
- 観察期間:12か月間
📊【主な結果】
- 薬剤曝露率:98.9%(良好なアドヒアランス)
- 心不全悪化の兆候なし(12か月間にわたって)
- バイオマーカーの変化:
- エナラプリル→ARNI群では:
- BNP↑、尿中cGMP↑(ネプリライシン阻害の反映)
- NT-proBNP↓(心負荷の軽減を示唆)
- 効果は2〜4週で出現し、12か月持続
- ARNIコア群では、すでに治療中であったため大きな変化は見られず
✅【結論】
- 日本人HFrEF患者において、ARNI(最大200mg BID)は1年間にわたり安全かつ良好に忍容された。
- NT-proBNPの持続的低下やBNP・尿cGMPの上昇は、ARNIの作用機序を反映しており、長期的な生理的反応と一致。
- この結果は、日本人におけるARNIの長期使用の安全性を裏付けるデータとなる。
🩺【臨床的意義】
- 日本人HFrEF患者に対しても、ARNIは長期投与可能で有効かつ安全であり、今後の実臨床での第一選択薬としての位置づけを支持する根拠となる。
メタ解析 https://pubmed.ncbi.nlm.nih.gov/30817783/
🧠【背景】
- 心不全治療ガイドラインでは、ACE阻害薬(ACEIs)、アンジオテンシン受容体拮抗薬(ARBs)、β遮断薬(BBs)を、主要なRCTで使用された「目標用量」まで増量することを推奨。
- しかし、高用量と低用量の間で有効性・安全性に実際どれほどの差があるかは明らかでなかった。
- 本研究は、HFrEF患者におけるそれら薬剤の高用量 vs. 低用量の効果とリスクを系統的に評価。
🔍【方法】
- *14件のRCT(~2–4年間の追跡)**を対象としたメタアナリシス。
- データベース:MEDLINE、Embase、CENTRAL、clinicaltrials.govなど
- 分析対象:
- 有効性指標:全死亡率、心血管死亡、全入院、心不全入院、心不全悪化
- 安全性指標:副作用、中止率、低血圧、めまい、高カリウム血症、腎機能障害
- 質評価:GRADE基準使用(ACEIs/ARBsは中等度~高、BBsは低~非常に低)
📊【主な結果】
【有効性】
| 指標 | ACEIs(高 vs. 低) | ARBs(高 vs. 低) | BBs(高 vs. 低) |
| 全死亡率 | RR 0.94(0.87–1.02) | RR 0.96(0.87–1.04) | RR 0.25(0.06–1.01)※低精度 |
| 全入院 | RR 0.94(0.86–1.02) | RR 0.98(0.93–1.04) | RR 0.93(0.39–2.24) |
| HF入院 | 有意差なし | RR 0.89(0.80–0.99)※有意 | – |
| HF悪化 | RR 0.85(0.79–0.92)※有意 | RR 0.91(0.84–0.99)※有意 | – |
※RR:相対リスク、95%CI:信頼区間
【安全性】
- 高用量群で副作用による中止率↑(3〜14%の絶対増)
- めまい・低血圧 → 全薬剤で↑
- 高カリウム血症・クレアチニン上昇 → ACEIs/ARBsで↑
- BBsに関しては結果が不明確かつ精度が低い
✅【結論】
- ACEIsとARBsの高用量は、心不全悪化リスクの軽減に有効。
- ARBs高用量は、HF入院リスクも有意に低下。
- ただし、死亡率や全入院の明確な改善効果は乏しく、精度にも限界。
- 高用量にすると副作用(特に血圧低下・腎機能障害)が増加。
- β遮断薬については、現時点のエビデンスは不十分。
🩺【臨床的意義】
- ACEIs/ARBsは忍容性を確認しながら慎重に増量すべき。
- 無理に最大用量を目指すのではなく、患者の忍容性を優先するバランスが必要。
- β遮断薬の増量に関する今後のエビデンスの蓄積が望まれる。
β遮断薬
HF-ACTION https://pubmed.ncbi.nlm.nih.gov/26519996/
🔍【研究の背景と目的】
- 慢性心不全(HFrEF)の治療において、β遮断薬(BB)の用量増加と心拍数(HR)の低下はどちらも予後改善と関連している。
- しかし、HRの低下とBB用量のどちらがより予後に貢献するかについては明らかでない。
- 本研究では、**HF-ACTION試験(NCT00047437)**のデータを用いて、BBの用量(カルベジロール換算)とHRの関連性を直接比較した。
🧪【研究デザイン】
- 対象:2,331人の外来慢性HFrEF患者(NYHA II~IV、LVEF<35%)
- 追跡期間:中央値2.5年
- 介入群:運動療法 vs 通常ケア(BB使用は観察的に評価)
- 評価項目:
- 主要評価:全死亡または全入院
- 副次評価:心血管関連アウトカム(心血管死、HF入院など)
📊【主な結果】
【未調整解析】
- BB高用量 → 予後改善(全死亡・入院リスク低下)
- 低HR(心拍数) → 同様に良好な傾向
- しかし、BB用量の方が一貫して強い効果
【多変量調整後】
- BB用量の効果のみが有意に残存
- HRの低下自体は、他の予後因子を調整すると有意性を失う
✅【結論】
- HFrEF患者においては、HRの低下よりもBBの高用量への漸増の方が予後改善に関連。
- BBは単にHRを下げる薬ではなく、用量依存的な有益な心筋リモデリング効果などがある可能性。
- 臨床的には、HRだけに注目するのではなく、BBを可能な限り耐容量まで増量する戦略が重要。
🩺【臨床的意義】
- 治療目標は「心拍数を下げること」ではなく、「BBを可能な限り最大耐容量まで増量すること」。
- HRが正常でも、BB増量によってさらなる予後改善が期待できる。
レビュー https://pubmed.ncbi.nlm.nih.gov/28521892/
🔍【背景】
- β遮断薬(β-blockers, BBs)は、HFrEF(駆出率低下型心不全)において死亡率および入院率を低下させる主要な薬剤。
- 初期は心拍抑制などからHFに有害と考えられていたが、現在は神経ホルモン系(交感神経)抑制作用を中心に、その有用性が確立。
- 近年では、「最大耐容量のβ遮断薬」投与が推奨されるが、その定義や実践の難しさが課題となっている。
📚【本レビューの目的と構成】
- β遮断薬の作用機序:HR低下だけでなく、神経ホルモン調整、心リモデリング改善に寄与。
- 主要RCT(MERIT-HF, COPERNICUS, CIBIS-IIなど)と現実臨床とのギャップ:
- 多くのRCTでは**目標用量(例:カルベジロール25–50mg BID、ビソプロロール10mg/dayなど)**が設定されていたが、
- 日常診療ではそれに達していない症例が多い(用量不足)
- BB増量を妨げる要因:
- 低血圧、徐脈、疲労感、うっ血悪化、医師の懸念など
- 治療目標としての「心拍数 vs. 用量」:
- 心拍数は重要だが、BBの予後改善効果は単なるHR低下以上の効果に基づく
- 心拍数だけを指標とせず、可能な限り最大耐容量まで増量を目指すことが重要
- 実臨床における推奨:
- 少量から開始し、2〜4週ごとに漸増
- HRや血圧、副作用を丁寧にモニタリング
- 高齢者や低体重者では柔軟な対応も必要だが、漫然と低用量で維持しない
✅【結論と提言】
- 「最大耐容量のBB」とは、副作用が出現する直前までの増量努力をした結果の投与量。
- HR低下だけを治療指標とするのではなく、RCTで示された有効用量を目指すことが真の治療目標。
- 用量漸増の戦略的アプローチと個別化を進めることで、さらなる予後改善が期待される。
🩺【臨床的意義】
- HFrEF管理において、β遮断薬は「可能な限り最大耐容量まで増量する」という明確な目標を持って投与すべき。
- 患者ごとに「耐えうる最大用量」の到達を目指すことで、心不全治療の質をさらに向上させる余地がある。
MRA
RALES試験
できるだけ早期に導入する
ACEi/ARB/ARNI
PIONEER-HF 試験 https://pubmed.ncbi.nlm.nih.gov/30415601/
🔍 研究の背景と目的
- 急性増悪した心不全(Acute Decompensated Heart Failure:ADHF)は、米国で年間100万件以上の入院の原因。
- 慢性心不全に対するARNI(サクビトリル/バルサルタン)の有効性は知られているが、ADHF入院中の導入が安全かつ有効かどうかは未解明。
- 本研究では、ADHF入院中にARNIを導入する有用性と安全性を、ACE阻害薬エナラプリルと比較して評価した。
🧪 研究デザイン
- 試験名:PIONEER-HF(NCT02554890)
- デザイン:多施設・無作為化・オープンラベル・盲検評価比較試験(PROBE法)
- 対象者:EFが低下(HFrEF)し、ADHFで入院・血行動態が安定した患者881名
- サクビトリル/バルサルタン群:440名
- エナラプリル群:441名
- 主要評価項目:NT-proBNP(心不全バイオマーカー)のベースラインから8週までの時間平均比の変化
- 安全性評価項目:腎機能悪化、高カリウム血症、症候性低血圧、血管浮腫
📊 主な結果
| 評価項目 | サクビトリル/バルサルタン群 | エナラプリル群 | 統計的有意差 |
| NT-proBNPの変化率 | -46.7% | -25.3% | P<0.001(有意) |
| 効果発現時期 | 1週目から明らか | – | – |
| 腎機能悪化 | 同等 | 同等 | 差なし |
| 高カリウム血症 | 同等 | 同等 | 差なし |
| 症候性低血圧 | 同等 | 同等 | 差なし |
| 血管浮腫 | 同等 | 同等 | 差なし |
✅ 結論
- サクビトリル/バルサルタンは、ADHF入院中の導入においてもエナラプリルよりも有意にNT-proBNPを低下させた。
- 安全性もACE阻害薬と同等であり、入院中からARNIを導入することは有望な治療戦略である。
🩺 臨床的意義
- 本試験は、急性期心不全の入院中からARNIを開始しても安全かつ効果的であることを示した初のRCT。
- 慢性期のみならず、急性期からの早期導入により、より迅速なリモデリング改善や予後改善が期待できる。
SGLT2i
EMPULSE 試験
入院中の強化GDMT戦略
STRONG‑HF 試験
そのためには、
- 副作用の早期発見と早期対処
- 併存疾患を考慮した薬剤選択